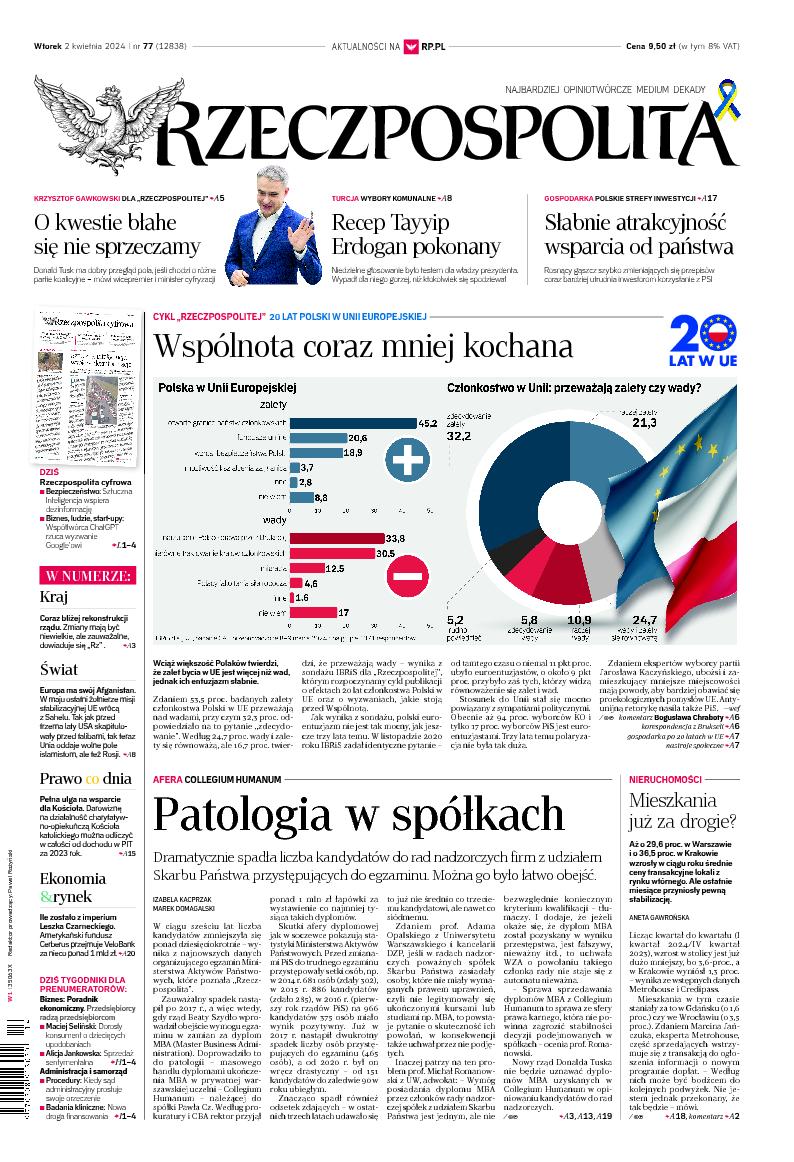
Nowa droga finansowania
Wdrożenie nowych przepisów ustawy o badaniach klinicznych to szanse dla administracji, pacjentów oraz zielone światło dla innowacji.
W ostatnim czasie, zarówno na gruncie prawa unijnego, jak i krajowego, można zaobserwować intensyfikację działań legislacyjnych, dotyczących badań klinicznych oraz dostępności do nowych leków. Potrzeba wzmocnienia konkurencyjności badań klinicznych w UE wymagała ujednolicenia i przejrzystości przepisów, które mogą zapewnić bezpieczne i konkurencyjne prowadzenie badań klinicznych.
Wyzwania dla administracji
Nowe zagrożenia epidemiologiczne czy choroby cywilizacyjne uznać możemy za przykładowe wyzwania, z którymi mierzy się administracja publiczna. Celem egzemplifikacji przywołajmy chociażby pandemię Covid-19. Kwestia dostępu do nowych innowacyjnych produktów leczniczych to poza ochroną zdrowia, również bezpieczeństwo państwa.
Od niedawna obowiązuje w Polsce ustawa z 9 marca 2023 roku o badaniach klinicznych produktów leczniczych stosowanych u ludzi, która umożliwiła...
Archiwum Rzeczpospolitej to wygodna wyszukiwarka archiwalnych tekstów opublikowanych na łamach dziennika od 1993 roku. Unikalne źródło wiedzy o Polsce i świecie, wzbogacone o perspektywę ekonomiczną i prawną.
Ponad milion tekstów w jednym miejscu.
Zamów dostęp do pełnego Archiwum "Rzeczpospolitej"
ZamówUnikalna oferta

![[?]](https://static.presspublica.pl/web/rp/img/cookies/Qmark.png)